Leucotrieno B4
O tema Leucotrieno B4 tem sido objeto de debate e estudo há anos, gerando opiniões conflitantes e teorias diversas. Desde a antiguidade, Leucotrieno B4 tem desempenhado um papel fundamental em diversos aspectos da vida humana, influenciando o desenvolvimento da sociedade, da cultura, da política e da economia. Ao longo da história, Leucotrieno B4 tem sido objeto de análise e reflexão, gerando inúmeras interpretações e discussões sobre o seu verdadeiro significado e o seu impacto no mundo atual. Neste artigo iremos explorar as diversas facetas de Leucotrieno B4, analisando a sua importância e relevância nos dias de hoje, bem como a sua influência em diferentes áreas da vida quotidiana.
| Leucotrieno B4 | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Nomes | |||||||||||||||||
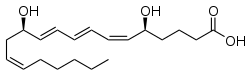
| Nome IUPAC | (5S,6Z,8E,10E,12R,14Z)-5,12-Dihydroxy-6,8,10,14-icosatetraenoic acid | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
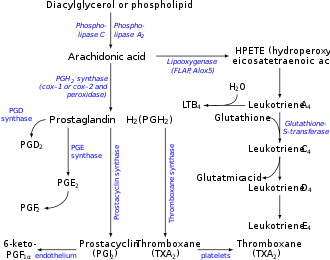
Leucotrieno B4 é um dos leucotrienos envolvidos no processo de inflamação. É produzido a partir de leucócitos em resposta a mediadores inflamatórios e é capaz de induzir a adesão e ativação de leucócitos no endotélio, que lhes permite ligarem-se e atravessar o tecido.[1]Em neutrófilos, também é um quimioatrator potente, e é capaz de induzir a formação de EROs (Espécies Reativas de Oxigênio) e a libertação de enzimas do lisossomo por estas células.[1] É sintetizado por meio da enzima leucotrieno-A4-hidrolase do leucotrieno A4.[2] [3]
Referências
- ↑ a b Cotran; Kumar, Collins. Robbins Pathologic Basis of Disease. Philadelphia: W.B Saunders Company. ISBN 0-7216-7335-X
- ↑ http://www.uniprot.org/uniprot/P09960. Consultado em 2 de Março de 2015 Em falta ou vazio
|título=(ajuda) - ↑ Rudberg PC, Tholander F, Andberg M, Thunnissen MM, Haeggström JZ (junho de 2004). «Leukotriene A4 hydrolase: identification of a common carboxylate recognition site for the epoxide hydrolase and aminopeptidase substrates». J. Biol. Chem. 279 (26): 27376–82. PMID 15078870. doi:10.1074/jbc.M401031200