Transformação isotérmica
Hoje, Transformação isotérmica é um tema de grande relevância e interesse na sociedade. O seu impacto reflete-se em diferentes áreas, da política à tecnologia, passando pela cultura e pela economia. Transformação isotérmica gerou discussões acaloradas, mudou a forma como as pessoas veem o mundo e desafiou estruturas estabelecidas. Neste artigo, exploraremos em profundidade a influência de Transformação isotérmica em nossas vidas e como ela moldou nossa percepção do mundo que nos rodeia. Desde as suas origens até ao seu impacto atual, Transformação isotérmica deixou uma marca indelével na sociedade moderna.

Uma transformação isotérmica é uma transformação termodinâmica que ocorre a temperatura constante em um sistema fechado, sistema este que permite trocas de energia, mas não de matéria, entre o sistema e sua vizinhança. Isto tipicamente ocorre quando o sistema está em contato com um reservatório térmico exterior (banho térmico), e a mudança ocorre lentamente o suficiente para permitir que o sistema se ajuste continuamente a temperatura do reservatório pelo meio de troca de calor. Em contraste, um processo adiabático é um sistema onde não há troca de calor com o meio externo (Q = 0). Em outras palavras, em um processo isotérmico, ΔT = 0, mas Q ≠ 0, enquanto que em um processo adiabático, ΔT ≠ 0, mas Q = 0.
Gás Ideal
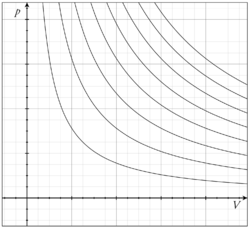
Para o caso especial de um gás perfeito, onde se aplica a Lei de Boyle-Mariotte, o produto PV é uma constante, se o gás for mantido em condições isotérmicas. O valor da constante é nRT, onde n é o número de mols de gás presente e R é a constante dos gases perfeitos.
Formalismo
Em termodinâmica, o trabalho envolvido quando um gás passa do estado A para o estado B é simplesmente:
Para uma transformação termodinâmica com a temperatura constante o trabalho de para (vide a figura no canto superior a direita) se dá da seguinte forma:
Obs.: Uma vez que a temperatura () é constante ela pode ser retirada da Integral.
O sinal do trabalho vai depender dos casos em que ele for:
- Se for uma expansão isotérmica o trabalho é positivo, pois , logo o logaritmo natural vai ser maior que 1. O logaritmo natural de um número maior do que 1 é positivo e, portanto, como era de se esperar, o trabalho é positivo;
- Se for uma compressão isotérmica, , de modo que a razão dos volumes é menor que 1. O logaritmo natural de um número menor que 1 é negativo e, portanto, o trabalho é negativo.
É também de notar que, em muitos sistemas, se a temperatura é mantida constante, a energia interna do sistema, também é constante, e assim . Da Primeira Lei da Termodinâmica, . Então, para processos isotérmicos. Em um caso especial, quando nenhum calor é trocado pelo sistema e a temperatura é constante, então não há trabalho realizado. Assim, o .
Referências
- HALLIDAY, D., RESNICK,R., WALKER, J., Fundamentos de física. 8ª edição, vol. 2, editora LTC.
Ver também
Nota: Este artigo contém trechos traduzidos do correspondente na Wikipédia em Inglês.












